La producción de metanol desde CO2, un paso más cerca
Frente a las emisiones de dióxido de carbono (CO2) hay una solución, capturar el gas y convertirlo en un combustible, como metanol. Científicos de la Universidad de California del Sur han encontrado un catalizador que facilita la reacción química necesaria para ese fin
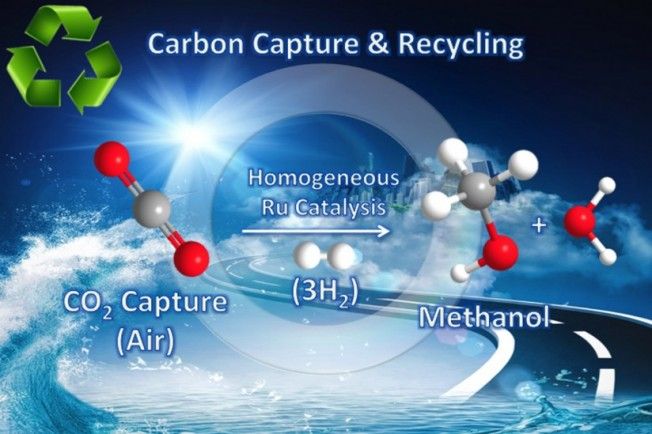
Esquema de la reacción que transforma CO2 en CH3OH
Los profesores de química de la Universidad de California del Sur G. K. Surya Prakash y George A. Olah (este último Nobel de Química en 1994) han conseguido acercar la posibilidad de generar combustible sintético, metanol (CH3OH) a partir del dióxido de carbono. Este combustible es una alternativa a la gasolina de origen fósil.
Hasta la fecha, el proceso para conseguir metanol a partir del CO2 era poco eficiente. La reacción química necesita altas temperaturas y el catalizador que la permite acababa consumiéndose por encima de los 150 ºC. Por lo tanto, el rendimiento de la reacción dista de ser satisfactorio para explotaciones a gran escala.
El metanol es el hidrocarburo más sencillo posible
La investigación de Surya Prakash y Olah ha dado como resultado un catalizador que resiste los 150 ºC de la reacción, incluso temperaturas superiores, sin consumirse, por lo que puede reutilizarse hasta cinco veces con un rendimiento aceptable. Así, es posible capturar el 79% del CO2 y convertirlo en metanol, aunque disuelto en agua. Para separar el agua del metanol basta un simple proceso de destilación.

Entrando más en detalle, los científicos introdujeron aire común en una solución acuosa de Pentaetilenohexamina (C10H28N6). El catalizador, junto a una temperatura 125-165 grados, rompe los enlaces covalentes del CO2 y logra la mezcla entre metanol y agua. El proceso industrial basado en este descubrimiento aún está a 5-10 años de distancia, se ha reproducido en laboratorio.
Los detalles del trabajo están disponibles en el Journal of the American Chemical Society del 29 diciembre de 2015. El proceso se tiene que perfilar para su utilización a escala industrial. Respecto a los procedimientos actuales, la novedad radica en una menor temperatura de reacción, por lo que hace falta menos energía.
Cuando esté perfilado el método de producción, bastará una fuente de energía renovable y aire común para la producción de metanol. Si bien es difícil producir cantidad suficiente como para reemplazar el consumo de gasolina, es una ayuda para el planeta. Será económicamente más rentable cuando el barril de petróleo vuelva a subir.

Muy pocos coches pueden utilizar metanol puro, como una versión del Fiat Panda. Los motores de gasolina pueden usarlo si se mezcla en pequeñas cantidades
El metanol no solo tiene utilidad como sustitutivo de la gasolina, también tiene aplicaciones en la industria química para la producción de etileno y propileno, destinados a la producción de plásticos. El método consigue matar dos pájaros de un tiro.
Esta técnica se llama ETL, Emissions To Liquid
No solo se produce una disminución -aunque muy pequeña de la concentración de CO2 en la atmósfera, también se consigue un combustible totalmente renovable y potencialmente infinito. Además, las emisiones contaminantes al usar metanol son muy inferiores a las de la gasolina de origen fósil.
Los combustibles sintéticos son otra de las posibles soluciones para hacer frente a la futura escasez del petróleo, a la vez que se reduce el efecto invernadero, relacionado con la concentración creciente de CO2 en la atmósfera por la mano del hombre. Dicha concentración ha ido creciendo desde el inicio de la revolución industrial, hasta 400 partes por millón (PPM).

Planta de producción de metanol George Olah (Islandia)
La experiencia islandesa
En Grindavik (Reykjanes, Islandia) se encuentra la mayor planta de producción de metanol sintético del mundo, y también fue la primera. Las obras comenzaron en octubre de 2009 y finalizaron en abril de 2012. La instalación tuvo un coste de 8 millones de dólares. La planta se llama George Olah, en honor al científico.
La planta produce un millón de litros de metanol por cada 1,1 miles de toneladas de CO2
La planta se alimenta de energía geotérmica, por lo que no produce emisiones contaminantes. El residuo del proceso es simplemente oxígeno, una especia de fotosíntesis artificial. El metanol producido se mezcla con la gasolina, en cumplimiento con la normativa comunitaria, que exige combustibles con una fracción de origen renovable hasta un 3%.
Como el metanol es biodegradable, tiene más octanaje y menos inflamable que la gasolina, la manipulación del combustible es más segura. Para su uso en automoción no implica riesgo alguno, es más, las cámaras de combustión del motor lo agradecen: la combustión es más completa y homogénea, y por el tubo de escape sale un aire un poco más limpio.

